脲酶的動力學(xué)研究
一、實驗?zāi)康?br style="box-sizing: border-box;"/>1.了解酶動力學(xué)的研究的一般內(nèi)容及方法。
2.掌握脲酶的動力學(xué)研究的操作步驟。
二、實驗原理
本實驗以脲酶(Mrease)為例研究底物濃度、pH、抑制劑(磷酸根離子)濃度對反應(yīng)速度的影響,并學(xué)會計算Km、V 等常數(shù)。
脲酶廣泛分布于植物界的種子中,某些微生物中也有,但在刀豆和大豆中含量較豐富。脲酶特異性地促使脲水解釋放出氨和二氧化碳,其反應(yīng)如下: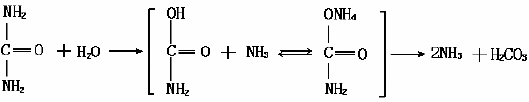
脲酶屬于一種寡聚酶44,分子量約為483000,等電點為4.8,最適pH 7.0。脲酶的Km 值因其來源不同和測定條件不同而異,例如刀豆脲酶,用pH7.0Tris-硫酸緩沖蔽,Km 為5.1×10 -3 MoL/L;本實驗是用大豆脲酶粗制品,pH7.0 Tris-硫酸緩沖液,25℃保溫,所測Km 值約為3.0×10 -3 mol/L 左右。
通過測定氨的釋放速度,就可得知水解速度。文獻(xiàn)中多采用奈氏(Nessler)試劑顯色法測定所釋放的氨量。其反應(yīng)如下:
由于該方法手續(xù)較繁,試劑也較貴,我們只用奈氏試劑作酶活力初步鑒定,而以康維(Conway)
微量等溫蒸餾定氨法測定氨量。
三、 儀器 和試劑
儀器
秒表、康維皿、細(xì)玻棒、恒溫水浴、恒溫箱、微量水平滴定管、吸量管。
實驗原料:新鮮大豆粉
試劑
1. 30%乙醇(V/V)
2. 人造浮石:Permutite 顆粒狀人造浮石。
3. 2%乙酸
4. 0.1mol/LpH7.0 Tris-硫酸緩沖液:取25mL2mol/LTris 溶液,加21mL0.1mol/L 硫酸,用水定容到50mL,檢查pH。
5. 3%脲-5.4%磷酸氫二納—4.25%磷酸二氫鉀溶液
6. 奈氏(Nessler) 試劑 :稱取5g 碘化鉀,溶于5mL 蒸餾水中,加入飽和氯化汞溶液(100mL 水約溶解
5.7g 氯化汞),并不斷攪拌,直至產(chǎn)生紅色沉淀不再溶解時.再加40mL50%氫氧化鈉溶液,稀釋至100mL,混勻,靜置過夜,傾出清液貯存于棕色瓶中。
7. 0.020mol/L、0.040 mol/L、0.060mol/L、0.080 mol/L、0.10 mol/L、0.16 mol/L 脲溶液。
8. 0.1mol/L、0.4mol/L、0.8mol/LPH7.0磷酸鹽緩沖液。
9. 0.1mol/L,pH5.0、pH6.0、pH7.0、PH8.0、PH9.0Tris—硫酸緩沖液。
10. 0.02 mol/L 準(zhǔn)硫酸銨溶液
11. 微量等溫蒸餾定氨所用試劑
12. 1mol/L 鹽酸
北京天優(yōu)福康生物科技有限公司
官網(wǎng):http://m.jyzjsd.com/
服務(wù)熱線:400-860-6160
聯(lián)系電話/微信:13718308763
QQ:2136615612 3317607072
E-mail:Tianyoubzwz@163.com


